Publié le 15 mar 2010Lecture 5 min
L’imagerie morphologique dans la maladie d’Alzheimer
J. PARIENTE, Inserm Imagerie Cérébrale et Handicaps Neurologiques, UMR 825 ; Service de Neurologie - Unité de Neuropsychologie, CHU Purpan, Toulouse
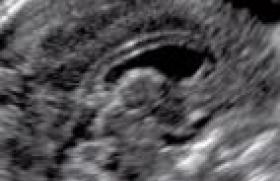
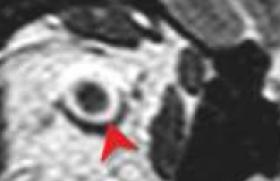
Comme cela est recommandé par la Haute Autorité de santé, une imagerie morphologique doit être réalisée lors du diagnostic d’une maladie d’Alzheimer (MA) : « Cet examen est une imagerie par résonance magnétique nucléaire (IRM) avec des temps T1, T2, T2* et Flair et des coupes coronales permettant de visualiser l’hippocampe » (1).
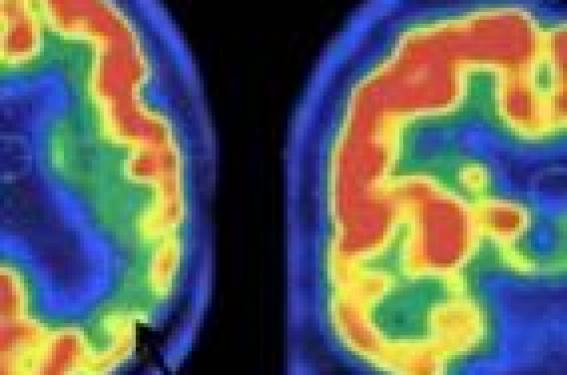
Une, deux, trois raisons... Il y a trois raisons pour réaliser ce type d’imagerie dans la MA. Il s’agit tout d’abord de rechercher des arguments en faveur du diagnostic, c'est-à-dire de rechercher une atrophie dans les régions temporales internes (images en séquence T1 avec des coupes coronales) ou au niveau cortical. D’autre part, cette imagerie peut mettre en évidence des lésions cérébrovasculaires constituant une comorbidité à la maladie dégénérative : petits infarctus sous-corticaux, lésions de leucoencéphalopathie ou microsaignements (microbleeds). Cette découverte aura une influence sur la prise en charge des facteurs de risque cardiovasculaires (images en séquence T2 et Flair pour les lésions ischémiques et T2* pour les lésions hémorragiques). Enfin, l’imagerie structurale permet d’éliminer ce qui était appelé autrefois, de manière abusive, une « démence curable ». Il s’agit en fait de rechercher des causes rares d’altération neuropsychologique non neurodégénérative (pas toutes « curables », en fait) : hydrocéphalie, tumeurs, hématomes sous-duraux, infarctus corticaux… Alors que la recherche de causes rares et de lésions cérébrovasculaires est relativement simple en IRM grâce aux séquences recommandées, identifier une zone d’atrophie est parfois plus complexe. Cette analyse peut être qualitative (c'est-à-dire visuelle) en se basant sur un examen antérieurement réalisé, et en se référant à des échelles d’atrophie peu pratiques en clinique ; ou de manière empirique, en fonction d’un a priori sur la taille d’un hippocampe normal. Cette analyse peut également être quantitative, mais n’est pas encore réalisée en pratique clinique courante. Vers un diagnostic personnalisé C’est un des paradoxes du diagnostic de la MA : de très nombreux travaux ont montré une corrélation entre atrophie hippocampique et altération mnésique (quel que soit le stade de la maladie) (2-4), d’où l’intérêt de l’IRM sur le plan diagnostic. PET scan au FDG d’un patient porteur d’une maladie d’Alzheimer. Hypométabolisme pariétal à gauche, temporal interne à droite. Mais à ce jour, il n’est pas possible encore d’extraire quantitativement ces informations en vue d’un diagnostic individuel. Cette dernière approche recommandée dans les « nouveaux critères de recherche de la maladie d’Alzheimer » (5) est détaillée ici. De nombreuses équipes à travers le monde et particulièrement en France se sont en effet attelées à lever ce « verrou technologique » (6-8). La manière semi-automatique Dans un travail récent, Chupin et coll. ont montré qu’il était possible de calculer de manière semi-automatique le volume de l’hippocampe grâce à un logiciel spécifique (9). Cette technique permet de « classer » correctement les patients MA sans a priori clinique dans 84 % des cas (sensibilité et spécificité de 84 %). Le même groupe a montré une différence significative entre les volumes hippocampiques de sujets sains, de patients ayant un trouble cognitif léger (MCI : Mild Cognitive Impairment) et de patients souffrant d’une MA, tout en notant qu’il existait un recouvrement des volumes hippocampiques entre ces trois groupes (8). Le suivi au fil des ans D’autre part, il est possible de suivre au fil des différentes IRM, l’atrophie dans cette région spécifique pour un patient donné, de nombreux travaux ayant montré que le taux d’atrophie annuel dans les régions temporales internes était plus important chez les patients atteints d’une MA comparativement aux sujets contrôles (10,11). Mais ce type d’approche pose un a priori sur les régions hippocampiques, alors que les études d’anatomopathologie montrent que les lésions spécifiques de la maladie commencent dans les régions sous-hippocampiques (cortex entorhinal), puis dans les régions hippocampiques, pour ensuite toucher d’autres régions temporales externes puis pariétales (12). Il paraît donc licite dès la phase symptomatique (même à un stade prédémentiel) de la maladie de s’intéresser à l’ensemble des régions corticales. Et la technique automatisée à 100 % Dans ce cadre, notre groupe a développé une technique totalement automatisée, rapide (15 minutes) permettant une aide au diagnostic à l’échelle individuelle. Le but de cette technique est de classer les patients en groupe MA/non MA en se basant sur une segmentation automatique du ruban cortical, puis sur le calcul de son épaisseur et d’un index d’atrophie (NTI : Normalized Thickness Index). Ce type d’analyse permet de différencier les patients atteints d’une MA à un stade démentiel versus des témoins dans 85 % des cas. La même technique a été appliquée à un groupe de patients « MCI » regroupant des patients porteurs d’une MA à un stade prédémentiel, mais également d’autres patients ayant un trouble de la mémoire d’une autre origine. Cette analyse permet à l’échelle individuelle de détecter de manière plus fiable l’évaluation neuropsychologique classique des patients qui évolueront vers un stade démentiel de la MA à 2 ans (7). « Toujours prêt ! » L’enjeu de ces techniques de morphométrie est capital dans le cadre du diagnostic de la maladie. Augmenter la spécificité du diagnostic est primordial car les traitements potentiellement efficaces sur le cours évolutif de la maladie auront des effets secondaires. Cette technique pourrait également trouver un intérêt dans le suivi des traitements, sans pouvoir pour l’instant se substituer à des critères principaux de jugements cliniques (cf. étude ancillaire de neuroimagerie dans la vaccination anti-Abêta42 (14-16)). Pour toutes ces raisons de spécificité, de précocité du diagnostic, de suivi évolutif, il faut se tenir prêt et utiliser au mieux ces techniques d’imagerie toujours de manière combinée avec la clinique, et parfois avec l’imagerie métabolique, et bientôt avec l’imagerie moléculaire.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :