Publié le 14 avr 2009Lecture 19 min
Imagerie cérébrale dans la sclérose en plaques : les avancées
M. VLAICU BUSTUCHINA, Service de Neurologie Hôpital Saint-Joseph, Paris ; Service de Neurochirurgie, Hôpital Pitié-Salpêtrière, Paris
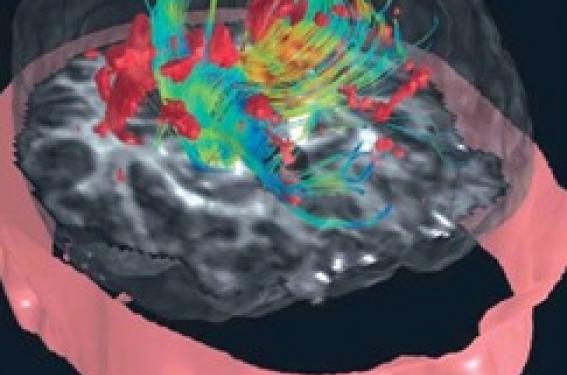
Au cours de ces 10 dernières années, l’imagerie par résonance magnétique (IRM) s'est imposée comme la méthode d'imagerie de référence pour le diagnostic de la sclérose en plaques (SEP). De plus, elle joue un rôle croissant dans la recherche scientifique et clinique sur cette maladie. La charge lésionnelle et le caractère inflammatoire peuvent être appréciés sur l’IRM anatomique. Cependant, l’IRM conventionnelle ne présente qu’une faible sensibilité et ne montre que peu de corrélation avec l'état clinique. De nouvelles approches, plus prometteuses, ont récemment vu le jour ou sont en cours de développement : ce sont ces nouvelles techniques et leurs apports que nous allons aborder ici.
Qu’il s’agisse des nouvelles utilisations de l’IRM conventionnelle, de l’IRM de tenseur de diffusion, de l’IRM de perfusion, de la spectroscopie par résonance magnétique à protons (1H-MRS)..., tous ces progrès en matière d’imagerie par résonance magnétique devraient améliorer notre capacité à diagnostiquer, à surveiller et à comprendre la physiopathologie de la SEP. En ce qui concerne le diagnostic, les principaux changements au cours des dernières années sont allés vers la simplification des critères, afin qu'ils deviennent plus faciles à manier. L’utilisation en pratique de ces nouveaux critères, récemment révisés, concourt à un diagnostic plus rapide et fiable, avec une meilleure sensibilité, tout en conservant une bonne spécificité. Avec ces nouveaux critères, l'utilisation de produit de contraste n’est plus nécessaire (1,2,3) (tableau 1). Nouvelles utilisations de l'imagerie conventionnelle Une meilleure approche de l’atrophie cérébrale Figure 1. Gain (rouge) ou perte (bleu) de volume cérébral déterminés à partir de séries d’IRM (voxel morphométrie). A : peu d'atrophie (0,29 % du volume de perte du cerveau par an). B : taux élevé d'atrophie (2,2 % du volume de perte du cerveau par an). Outre l’identification des lésions, l'imagerie conventionnelle mesure l'étendue de l'atrophie cérébrale. Déterminer la topographie et le taux d'atrophie cérébrale chez les patients atteints d’une SEP, constitue un domaine d’intérêt, qui au cours des dernières années, ne cesse de croître. Chez les patients atteints de sclérose en plaques, la perte de tissu semble être plus importante au niveau de la substance grise que de la substance blanche. Apparemment, les ganglions de la base et le thalamus sont plus sensibles à l’atrophie (4). L'une des causes de la mauvaise classification des lésions de la substance blanche et de la substance grise est probablement l’utilisation d’une correction manuelle. Les nouvelles méthodes disponibles pour déterminer l’atrophie régionale de la substance grise, entièrement automatisées (voxel morphométrie et segmentations semi-automatiques) vont améliorer certainement les résultats (5) (figure 1). La segmentation des images de soustraction (SSEG) comparée à la segmentation classique (CSEG) constitue un outil prometteur pour fournir une analyse détaillée à propos de modifications subtiles de la taille et de l'intensité des lésions. La SSEG peut offrir d'autres éclaircissements sur les modes de progression de la SEP (6). Les variations de volume du cerveau ont été étudiées récemment chez des patients qui ne présentaient pas tous la même forme de SEP et ne se trouvaient pas tous au même stade de la maladie6. Il apparaît ainsi que l’atrophie s’accentue de manière constante tout au long de l’évolution de la SEP. Des études récentes ont montré une diminution de volume cérébral après l’utilisation de différents traitements : immunomodulateurs, corticothérapie, natalizumab, interféron bêta (7,8). Les changements à court terme pourraient être en partie expliqués par un effet osmotique et anti-inflammatoire, dénommé pseudo-atrophie. Davantage d’études sont nécessaires pour nous aider à distinguer la véritable atrophie d’une possible pseudo-atrophie pour essayer de comprendre la relation entre démyélinisation, perte neuronale ou axonale, neurodégénérescence et modification du volume cérébral. L’IRM de la moelle Chez les patients atteints d’un syndrome clinique isolé, la valeur de l'IRM conventionnelle de la moelle épinière a été officiellement reconnue internationalement et acceptée dans les critères diagnostiques. Les progrès techniques se sont principalement axés sur l'imagerie de la portion cervicale de la moelle (9). Davantage d'efforts devraient être consacrés à l'amélioration de l'IRM de l'ensemble de la moelle (10). Les techniques d’imagerie « non conventionnelles » L’IRM de tenseur de diffusion (DTI) Pour évaluer la progression de la maladie, on a besoin d’analyser d’autres paramètres comme, par exemple, les degrés de démyélinisation et/ou de neurodégénérescence, qui constituent des marqueurs des processus pathologiques liés à la SEP. Discerner indirectement la position, l’orientation et l’anisotropie des faisceaux de la substance blanche du cerveau est actuellement possible grâce à l’IRM de tenseur de diffusion. La DTI fournit des informations sur l’organisation des tissus à travers plusieurs paramètres. On s’intéresse ainsi au coefficient de diffusion apparent (ADC) et à la fraction d’anisotropie (FA) (11). Dans les plaques et dans la substance blanche d’apparence normale, il existe une augmentation du coefficient de diffusion apparent et une diminution de la fraction d’anisotropie. En mesurant les diffusivités axiale et radiale par comparaison aux valeurs de FA et d’ADC, quelques études ont essayé de mieux caractériser les différentes formes cliniques de la SEP (12). L'IRM de tenseur de diffusion permet à la fois d'étudier les faisceaux des fibres nerveuses et de différencier l'atteinte de l'axone de l'atteinte de la myéline. Avec cette technique, on peut déduire l'orientation des axones, et reconstruire le parcours des principaux faisceaux de la substance blanche (13). Ainsi, l’IRM de tenseur de diffusion constitue-t-il un outil sensible pour la caractérisation physiopathologique de la sclérose en plaques et potentiellement pour le suivi clinique des patients. L'IRM de tenseur de diffusion permet à la fois d'étudier les faisceaux des fibres nerveuses et de différencier l'atteinte de l'axone de l'atteinte de la myéline. En associant une couleur à chacune des trois directions de l’espace : rouge pour gauchedroite, bleu pour crânio-caudale, vert pour antéro-postérieur, on obtient une cartographie des faisceaux indiquant leurs positions, directions et anisotropie. En utilisant la tractographie 3D (14) (figure 2), on peut visualiser les faisceaux des fibres de substance blanche, et ainsi mieux caractériser l’intégrité axonale. Dans quelques études, l’IRM de tenseur de diffusion a été utilisée pour évaluer la relation entre le profil cognitif de la sclérose en plaques bénigne et l’étendue des lésions des tissus du corps calleux (15). Il est ainsi apparu que le dysfonctionnement cognitif est associé à une augmentation des anomalies du corps calleux (16). Figure 2. A : DTI (IRM de tenseur de diffusion) : la surface « transparente » du cerveau permet de visualiser la localisation des lésions (en rouge) à partir d'une image pondérée en T2. La tractographie 3D fait apparaître les faisceaux dans la substance blanche. B : Tractographie du tractus corticospinal. Alors que les modifications de la substance blanche hippocampique chez les patients souffrant d’une SEP sont difficiles à visualiser avec une IRM conventionnelle, l’IRM de tenseur de diffusion est capable de mettre en évidence les modifications hippocampiques (17). Le fornix, principal efférent de l'hippocampe, intimement lié à la fonction de mémoire, se prête particulièrement bien à un examen par l’IRM de tenseur de diffusion. Le déficit en mémoire épisodique semble fortement corrélé avec les modifications du fornix. Ainsi, ces modifications visualisées par l’IRM de diffusion pourraient être considérées comme un « marqueur » de dysfonctionnement de la mémoire épisodique dans la SEP (18). Méthode de soustraction L'utilisation d'une méthode de soustraction d'imagerie montre l'évolution des lésions de la SEP dans le temps avec une sensibilité accrue par rapport à l'analyse qualitative (figure 3). L’IRM double inversionrécupération (DIR) Cette technique est particulièrement intéressante pour la détection des lésions corticales (19). Grâce à elle, on peut visualiser les lésions de la substance grise et tenter d’établir une corrélation avec l’atrophie corticale et les éventuels troubles cognitifs. L'IRM de perfusion L'évaluation de la perfusion des tissus du cerveau in vivo est désormais possible grâce à l’IRM de perfusion (figure 4). Dans la SEP, les lésions aiguës se signalent par une augmentation de la perfusion, alors que la substance blanche normale et la substance grise sont le siège d’une diminution de la perfusion. La sclérose en plaques est caractérisée par des zones de démyélinisation inégales dans l'ensemble de la substance blanche d’apparence soi-disant normale (NAWM) (inflammation, perte axonale, gliose, dégénérescence axonale diffuse). Figure 3. Méthode de soustraction de l'image. Patiente de 44 ans avec une SEP récurrente-rémittente au début (A) et à 3 ans (B et C). Une nouvelle lésion juxtacorticale (flèche) est clairement visible avec la soustraction d'image (C). Un certain nombre d'études récentes utilisant l'imagerie par résonance magnétique de perfusion dans les formes progressives de SEP ont montré une diminution de la perfusion NAWM, qui ne semble pas être secondaire à la perte axonale. Des phénomènes ischémiques pourraient être impliqués dans le développement d'un sous-type de lésions démyélinisantes (lésions de type III). Cette technique pourra être utilisée pour surveiller l'évolution de la maladie et l'efficacité du traitement, mais la sensibilité et la pertinence de l'IRM de perfusion dans la SEP doivent être encore prouvées par d’autres études (20). Des phénomènes ischémiques pourraient être impliqués dans le développement d'un sous-type de lésions démyélinisantes. L'imagerie à haut champ de sodium Dans des modèles expérimentaux de SEP, il a été démontré que le blocage partiel des canaux sodiques peut protéger contre la dégénérescence des axones. Actuellement, l'imagerie à haut champ de sodium (3,0 tesla), fournissant des images de haute qualité dans un temps d'acquisition acceptable, permet d’évaluer la viabilité des tissus en fonction de cette notion ; elle est pour l’instant seulement utilisée dans des essais cliniques (21). L’IRM du transfert d’aimantation L’IRM du transfert d’aimantation (Magnetisation transfer MRI, MTR) n’a été employée que dans un petit nombre d'essais et pour certains groupes de patients. Plus récemment, elle a été appliquée au suivi de la démyélinisation et de la remyélinisation dans les lésions de SEP. Figure 4. IRM coupe axiale (A) montrant le débit sanguin cérébral (B) et le volume (C) chez un patient atteint de SEP. Les barres de couleur indiquent l’importance du débit sanguin cérébral par minute (ml/100 g/min) et le volume sanguin cérébral (ml/100 g). Des approches fondées sur des atlas ont été utilisées dans des études longitudinales pour suivre l'évolution des anomalies au sein des lésions (MTR T2), ce qui devrait permettre d’élaborer des cartes pour classer les lésions par ordre chronologique. Des études préliminaires ont montré que cette technique fournit des indications pronostiques quant à l’évolution de la maladie. Elle pourrait également contribuer à mieux faire comprendre le processus d’apparition du handicap. Potentiellement, on peut en espérer une amélioration des corrélations avec les manifestations cliniques et de pouvoir suivre l'effet du traitement sur la réparation de la myéline et la neuroprotection. C’est un outil d’appoint paraclinique prometteur dans des études longitudinales. IRMf (BOLD) L’imagerie basée sur la technique BOLD (Blood oxygenation level dependent) est à l’origine de beaucoup de recherches en neurosciences. Elle trouve des applications dans l’évaluation des voies visuelles, des modifications fonctionnelles corticales et des troubles cognitifs dans la sclérose en plaques. Les anomalies structurales et fonctionnelles hippocampiques sont détectables dans la SEP en utilisant des techniques d'imagerie de haute résolution (22). Le suivi de ces anomalies peut être utile dans les études analysant le dysfonctionnement cognitif dans la SEP. Il est également possible d'intégrer les résultats de l’IRM de diffusion avec les données de l'IRM fonctionnelle et de la magnéto-encéphalographie pour mieux comprendre comment les différentes altérations au sein des lésions peuvent affecter les taux de transmission, la réserve fonctionnelle, les connexions cérébrales et la plasticité cérébrale (23). Ces recherches pourraient fournir un aperçu fascinant du statut neuronal, de la durée de l'inflammation, de la démyélinisation et de la remyélinisation, et l'impact qu'elles ont sur la fonction cognitive et motrice. 1H-MRS (spectroscopie IRM) Cette technique, autrefois réservée à la recherche, est entrée dans le bilan de routine des affections démyélinisantes. La technique 1H-MRS peut être utilisée pour mesurer les métabolites, tels que la N-acétylaspartate, la choline, la créatine, le myo-inositol. On sait déjà qu’une diminution de la N-acétyl-aspartate est associée à une atteinte axonale ou un dysfonctionnement neuronal, que la choline augmente au cours de la remyélinisation et de l'inflammation, que la concentration de créatine augmente avec la densité cellulaire, et enfin que l'augmentation de myo-inositol est évocatrice de la prolifération des cellules gliales (24). Les acides aminés, les neurotransmetteurs comme le glutamate, la glutamine et le GABA, peuvent également être mesurés24 (figure 5). Figure 5. Spectrographie IRM : lésion aiguë (A) ; lésion chronique (TE-averaged PRESS spectrum) (B). Les progrès de la spectroscopie par IRM devraient permettre la détection de nouveaux métabolites pertinents pour la SEP qui sont en cours d’étude (le glutathion, le GABA, l'acide ascorbique). Les macromolécules (valine, alanine, leucine, isoleucine, thréonine), qui représentent jusqu'à 60 % du contenu de la myéline, sont détectées par l’utilisation de l'inversion des séquences de récupération. La spectroscopie 3 tesla améliore la résolution spectrale par rapport au 1,5 tesla (24). La quantification d'un tel profil neurochimique large in vivo devrait aboutir à mieux comprendre le rôle de la neurodégénérescence, de la réparation tissulaire, de la thérapie antioxydante et du stress oxydatif dans la SEP. La SRM au phosphore La spectroscopie au phosphore montre que la phosphocréatine augmente dans la substance blanche en apparence normale. Il existe probablement dans la SEP une atteinte du métabolisme énergétique (25). Imagerie de la myéline La sclérose en plaques est caractérisée par des cycles de démyélinisation et de remyélinisation dans des zones localisées. Une technique reposant sur la relaxation T2 permet de distinguer trois compartiments avec un T2 long (correspondant au LCR), un T2 intermédiaire (attribué aux échanges intra- et extracellulaire de l'eau) et un T2 court (attribué à l'eau qui existe dans la myéline). L’histologie montre que l'eau dans la myéline est un marqueur spécifique de la myélinisation. Les modifications de la teneur totale en eau (WC) et de la fraction d'eau dans la myéline (MWF : myelin water fraction) au cours de l'évolution des lésions MS peuvent être mises en évidence par cette méthode et autoriser ainsi la surveillance de la démyélinisation et de la remyélinisation dans la SEP. Toutefois, ce type d’imagerie pose encore un défi technique (26). Les nouveaux agents de contraste Figure 6. Lésion aiguë chez un patient atteint de SEP. Différences d’image avec le gadolinium et les particules ultrafines d'oxyde de fer (USPIO). La lésion est hyperintense en T2 (A), mais n’est pas mieux visualisée avec l’injection de gadolinium T1 (B). Après l’injection d’USPIO (T2) (C), le renforcement USPIO conduit à une diminution de l'intensité du signal (T2). Toutefois, la lésion est renforcée après l'administration d’USPIO sur l'image pondérée en T1 (D). En IRM conventionnelle, en cas de plaques aiguës, la rupture de la barrière hémato-encéphalique se traduit par une prise de contraste lors de l'injection de gadolinium. La perte de lipides au niveau de la myéline et l'augmentation de l'eau libre au niveau des plaques de démyélinisation sont responsables de l'allongement du T1 et du T2. Il existe deux types de produits de contraste à base d’oxydes de fer superparamagnétiques en fonction de leur taille : les SPIO (Superparamagnetic iron oxide) à tropisme hépatique et les USPIO (Ultrasmall superparamagnetic iron oxide) à tropisme ganglionnaire. Ces nouveaux produits de contraste pour l’IRM ont été utilisés chez les patients atteints de sclérose en plaques (figure 6). Le marquage cellulaire de la substance blanche en apparence normale, qui est obtenu en utilisant ces produits de contraste, peut témoigner d’une inflammation cellulaire diffuse (27). Les informations fournies par le suivi des macrophages marqués avec les particules de fer pourraient aider à l’évaluation de l'efficacité de médicaments ciblant les éléments cellulaires de l'inflammation. D'autres responsables de l'inflammation ou le dysfonctionnement des neurones pourraient être visualisés par de nouveaux produits de contraste. L’activité de la myéloperoxydase dans l'inflammation des tissus peut être détectée in vivo (28). Une autre nouveauté, la gadofluorine M, s'accumule sélectivement dans les fibres nerveuses au cours de la dégénérescence wallerienne (29). Ce produit de contraste est à la fois hydrophobe et hydrophile. Il inverse le contraste en T1 (modèle d’EAE de rat) (30). Ces nouveaux agents de contraste ont besoin d’être validés et évalués quant à leur innocuité avant de déterminer leur place. L'IRM de champ supérieur à 1,5T À l’heure actuelle, la plupart des IRM s’effectuent sur des appareilles 1,5 tesla, et 3 tesla. L’imagerie en pondération T2 est améliorée à 3 tesla. Les IRM de haut champ (3,0T en général) et ultra-haut champ (≥ 7,0T) ont une valeur particulière pour détecter de façon très précise les petites lésions de sclérose en plaques, notamment dans les localisations juxtaventriculaires et intracorticales, et étudier de manière très fine l’hippocampe (31) (figure 7). Les IRM 3 tesla ou 4 tesla peuvent améliorer les autres techniques « non conventionnelles (l’IRM de diffusion, l’IRM de perfusion, la 1H-MRS, l'IRMf) ». En effet, on obtient pour la même séquence et pour le même temps d’acquisition une meilleure résolution spatiale. Il est ainsi possible de réaliser des acquisitions 3D en haute résolution dans des délais très courts. Les premières explorations réalisées chez l’homme avec le système 7 tesla ont permis d’obtenir des images de haute qualité concernant notamment le contraste entre la substance blanche et la substance grise (amélioré 10 fois) (32). Il est possible de faire une étude de la microvascularisation, mieux visualiser les structures cérébrales fines (imagerie dite « microscopique »), révéler de nouvelles structures au sein des fibres qui constituent la substance blanche. Des champs supérieurs à 1,5 tesla peuvent ainsi révolutionner la recherche dans la SEP. Par ailleurs, ils pourraient améliorer le diagnostic précoce de la MS. Autres modalités d’imagerie Les promesses de la TEP haute résolution La tomographie à émission de positons haute résolution offre de nouvelles perspectives pour la visualisation des lésions de destruction de la myéline et l’évolution de la réparation myélinique. Dans une étude utilisant le traceur flumazénil, il a été possible d’obtenir en TEP haute résolution un marquage neuronal (33). Les auteurs ont montré que les patients avec une SEP progressive ont une perte neuronale de 30 % dans les thalamus et de 10-15 % dans des régions corticales. Figure 7. Comparaison entre IRM 1,5T et IRM 3,0T chez deux patients avec une SEP. Une femme de 48 ans avec SEP secondairement progressive. A : IRM 1,5T, coupe axiale, FLAIR ; B : IRM 3,0T, coupe axiale, FLAIR. Un homme de 23 ans avec SEP récurrente-rémittente. C : IRM 1,5T (coupe coronale) ; D : IRM 3,0T (coupe coronale). Les images en 3,0T (B, D) de la même région améliorent la sensibilité dans les capacités de détection de la lésion (flèches) et de la différenciation entre la substance blanche et la substance grise. La tomographie en cohérence optique (TCO) L’imagerie des nerfs optiques est difficile parce qu'ils sont très petits et sujets aux artefacts de mouvement. Cependant, la névrite optique est un excellent modèle d'étude de la physiopathologie et de la réparation des dommages associés à la SEP. La tomographie en cohérence optique (TCO) constitue ici une méthode d’imagerie intéressante (34) (figure 8). Cette technique à l’infrarouge non invasive permet de mesurer l’épaisseur des fibres nerveuses de la rétine. D'importantes questions restent à résoudre quant à la physiopathologie de la névrite optique et l’intérêt de l'imagerie dans le suivi longitudinal. La technique 1HMRS a la possibilité de montrer à l'heure actuelle des changements inflammatoires, une gliose et la perte axonale. L'imagerie du tenseur de diffusion et l’imagerie de transfert de magnétisation ont la possibilité de faire la preuve de l'intégrité axonale et du contenu en myéline du nerf optique, mais il y a encore des obstacles techniques à surmonter. Conclusion Les progrès techniques récents et à venir en neuro-imagerie devraient améliorer la capacité à diagnostiquer et à contrôler la maladie, ainsi que la compréhension de la physiopathologie de la SEP. Les nouvelles méthodes d’IRM doivent encore être évaluées pour préciser leurs performances quant à la précocité du diagnostic. La signification fonctionnelle des lésions pourra être précisée par l’IRM de diffusion, avec également une meilleure compréhension des troubles cognitifs. L’imagerie de la myéline apporte un vrai espoir ; la spectroscopie par résonance magnétique, avec un champ plus élevé, devrait permettre la détection d'un éventail plus large de métabolites, et avec les nouveaux agents de contraste de résonance magnétique, l’imagerie cellulaire semble désormais possible ! La combinaison des diverses méthodes de résonance magnétique, qui explorent différents aspects de la pathologie dans le cadre de la SEP, est une voie prometteuse pour accroître notre compréhension des mécanismes sous-jacents à la progression vers le handicap irréversible. Dans l'avenir, il sera nécessaire de préciser dans quelle mesure ces progrès de la technologie d’IRM peuvent nous fournir des informations pertinentes, afin d'améliorer le pronostic et prédire la réponse thérapeutique (35). Les nouvelles techniques doivent encore être affinées et validées avant d'être intégrées dans la recherche clinique et dans la pratique. Figure 8. La tomographie – ou visualisation en profondeur – de la rétine est obtenue avec la tomographie optique cohérente (OCT).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :