Publié le 25 sep 2013Lecture 12 min
Neuropathies toxiques post-chimiothérapie
D. PSIMARAS*,***, D. RICARD*,**,*** * Service de neurologie Mazarin, Hôpital Pitié-Salpêtrière, Paris ** Service de neurologie, Hôpital d’Instruction des Armées du Val-de-Grâce, Paris *** Groupe OncoNeuroTox
Les neuropathies périphériques peuvent être secondaires au traitement de chimiothérapie ou de radiothérapie. Il est capital pour le clinicien de pouvoir reconnaître la neurotoxicité et de la distinguer d’autres complications inhérentes au cancer. Pour qu’elle soit efficace, la prévention doit prendre en compte la physiopathologie de ces mécanismes, adapter le traîtement utilisé et proposer des agents neuroprotecteurs encore en étude.
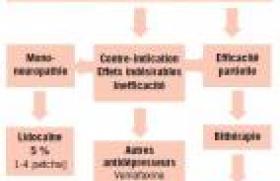
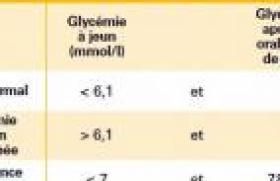
Les neuropathies (NP) chimio-induites se traduisent le plus souvent (NPCI) constituent une complication fréquente et invalidante de plusieurs traitements utilisés en oncologie. On connaît mal les mécanismes physiopathologiques en cause dans le développement de la NPCI. Il s’agit le plus souvent d’une polyneuropathie distale, longueur-dépendante à prédominance sensitive, s’exprimant cliniquement par une hyperexcitabilité nerveuse comprenant des dysesthésies, des paresthésies ou des douleurs. La nature de la neuropathie est drogue-dépendante ; il peut s’agir d’une neuropathie sensitive pure (exemple : la NPCI au cisplatine) ou mixte sensitivomotrice (exemple : la NPCI induite par la vincristine ou les taxanes). Sa détection précoce est capitale et peut conduire à une modification de la prise en charge thérapeutique néoplasique ultérieure afin de limiter ou faire régresser les désordres induits. La prévention de cette complication repose essentiellement sur la diminution ou l’arrêt des médicaments en cause ; elle tend à s’améliorer à l’arrêt du traitement, parfois de façon incomplète. Plusieurs agents neuroprotecteurs ont été utilisés, mais très peu ont montré une efficacité. L’incidence de la NPCI est en rapport avec la dose cumulative et la durée du traitement(1). Elle semble plus marquée l’association à des médicaments neurotoxiques, par exemple pour le cancers gynécologiques traités par taxanes et platines(2). Malgré l’impact clinique des NPCI, il n’existe pas encore d’outil d’évaluation diagnostique et de suivi clinique(3). Les échelles fonctionnelles les plus couramment utilisées dans la thématique, la NCI-CTC v.3 (National Cancer Institute-Common Toxicity Criteria) et l’échelle de l’OMS (Organisation mondiale de la santé) sont des échelles oncologiques qui ne permettent pas une évaluation précise de la neuropathie périphérique. L’échelle TNS (Total Neuropathy Score), qui combine une évaluation des symptômes et des signes d’examens simples, est actuellement de plus en plus utilisée dans les études cliniques et en pratique courante. Il s’agit d’une échelle créée pour l’évaluation de la neuropathie chez les patients diabétiques, qui semble plus spécifique sans perdre en sensibilité par rapport aux échelles du NCI(4). Cette échelle est actuellement en cours d’étude dans le cadre d’un travail européen dédié aux NPCI. Neurotoxicité des médicaments Nous allons détailler, ici, les caractéristiques des drogues pourvoyeuses de neuropathie périphérique(5) (tableau). Nous ne parlerons pas de la classe des alkylants (ex. : busulfan ou cyclophosphamide), des antimétabolites (capécitabine ou méthotrexate) et des modificateurs de l’ADN (ex. : irinotécan ou doxorubicine), car leurs effets secondaires sur le nerf périphérique sont inexistants ou anecdotiques. Inhibiteur du protéasome • Bortézomib Le bortézomib (Velcade®) appartient à la nouvelle classe thérapeutique des inhibiteurs du protéasome, qui a constitué ces dernières années un grand progrès dans le traitement du myélome multiple. Actuellement indiqué en deuxième intention, il est de plus en plus utilisé en première ligne, toujours associé à la dexaméthasone. Le principal effet secondaire limitant est la NP qui survient chez au moins un tiers des patients et qui est le plus souvent dose-dépendante. Il existe une bonne récupération clinique avec 71 % des patients présentant une amélioration à 2 mois de la fin du traitement. La préexistence fréquente d’une polyneuropathie (grade 1 ou 2) chez les patients avec myélome multiple (jusqu’à 15 % des patients) prédispose au même titre que le diabète au développement d’une polyneuropathie plus sévère (grade 3 ou 4). Il s’agit le plus souvent d’une polyneuropathie sensitive à l’examen, avec atteinte motrice cliniquement discrète mais fréquente sur le plan électrophysiologique. Quelques cas de polyneuropathies démyélinisantes à médiation probablement immune, ayant bien répondu au traitement spécifique par Ig IV, ont été décrits. Sur le plan physiopathologique, toutes les fibres nerveuses sont touchées et il semble qu’il existe une toxicité sur l’axone mais également sur le ganglion rachidien postérieur. La diminution des doses, de même que l’espacement des séances de traitement permettent souvent une amélioration de la symptomatologie neurologique. Des recommandations ont ainsi été établies pour adapter les doses en fonction de la survenue d’une neuropathie. Poisons du fuseau et stabilisateurs de membrane • Alcaloïdes de la pervenche Cette classe de molécules empêche la formation normale de la tubuline pour l’assemblage des microtubules au niveau du fuseau. Il existe trois principaux médicaments : la vincristine (Oncovin®), la vinblastine (Velbé®) et la vinorelbine (Navelbine®). Leur toxicité est essentiellement hématologique, mais atteint également le système nerveux périphérique. La vincristine est largement utilisée dans les leucémies, les lymphomes, les myélomes et certains sarcomes. Il s’agit d’une molécule ancienne qui induit une polyneuropathie axonale, sensitivomotrice, dose-dépendante. L’incidence en est estimée jusqu’à 57 % selon les séries, avec une réversibilité de la neuropathie dans 66 % des cas, mais souvent incomplète. Il est essentiel de discuter la poursuite du traitement dès l’apparition d’une gêne fonctionnelle d’origine sensitive (lâchage d’objet, écriture difficile) ayant un impact dans la vie quotidienne. Ces troubles sont lents à récupérer et précèdent généralement de peu la survenue d’une atteinte motrice parfois irréversible. L’interrogatoire du patient avant chaque administration de vincristine est donc essentiel. Des signes dysautonomiques sont très souvent présents et doivent être recherchés (hypotension orthostatique, gastroparésie). L’iléus peut le plus souvent être prévenu ou levé grâce à la prescription de péristaltine. Une prise en charge strictement médicale, avec mise en aspiration, est parfois nécessaire. Le recours à la chirurgie est exceptionnel. La vinblastine et la vinorelbine sont de moindre toxicité, et celle-ci se limitant à des paresthésies et une aréflexie sans déficit moteur. La toxicité dysautonomique est également observée avec la navelbine. Il existe une nouvelle molécule en étude actuellement, la vinflunine, qui serait beaucoup moins neurotoxique que les 3 autres, avec l’apparition d’une neuropathie dans seulement 12 % des cas. Elle a obtenu une AMM dans le cancer de la vessie en 2009. • Épothilones Elles constituent une nouvelle classe de stabilisateurs des microtubules, de mécanisme commun avec les taxanes, auxquels ils se substituent souvent comme traitement de deuxième intention, en particulier dans le cancer du sein métastatique. Les molécules le plus communément utilisées sont la patupilone et l’ixabépilone. Elles sont à l’origine de NP sensitives et souvent peu sévères. • Taxanes Le paclitaxel (Taxol®) et le docétaxel (Taxotère®) sont deux traitements utilisés essentiellement dans le cancer du poumon, du sein et de l’ovaire. Ils sont souvent prescrits en association avec les sels de platine entraînant alors des NP plus précoces et plus sévères(10). Ils présentent une toxicité nerveuse périphérique, longueur-dépendante, distale et symétrique. Cette toxicité est plus prononcée pour le paclitaxel (10-20 % des patients) que pour le docétaxel. Toutes les modalités sensitives peuvent être atteintes et les ROT sont précocement diminués. Des anomalies cliniques motrices sont souvent associées mais discrètes. La neuropathie aux taxanes est le plus souvent réversible ; des troubles sensitifs peu gênants peuvent cependant persister au long cours dans une minorité de cas. Sels de platine Les représentants de cette classe médicamenteuse sont le cisplatine (Cisplatyl® ou CDDP), l’oxaliplatine (Eloxatine®) et le paraplatine (Carboplatine®). • L’atteinte du SNP sous forme de neuropathies périphériques est la complication la plus fréquente La mieux décrite est l’atteinte par le cisplatine. Il s’agit d’une polyneuropathie sensitive pure (douleurs et dysesthésies) ataxiante par lésion ou perte de fibres de gros diamètre, survenant dans 30-40 % des cas. Il s’agit d’une polyneuropathie dose-dépendante qui survient durant le traitement (quasiment constante lorsque les doses cumulatives atteignent 900 mg/m2) et peut parfois s’aggraver dans les semaines suivant l’arrêt de la chimiothérapie (phénomène appelé « coasting »). Ce phénomène, assez caractéristique de la complication liée au cisplatine, a été également décrit avec le traitement par vincristine ou par taxanes. À terme, il existe une amélioration clinique dans deux tiers des cas, mais le plus souvent partielle. Le cisplatine est à l’origine d’une polyneuropathie dose-dépendante qui survient durant le traitement et peut parfois s’aggraver dans les semaines suivant l’arrêt de la chimiothérapie. • L’oxaliplatine est le plus récent des dérivés de platine Il est essentiellement utilisé dans les cancers colorectaux et induit une neuropathie périphérique chronique comparable au cisplatine, mais avec une moindre fréquence et une moindre sévérité. L’oxaliplatine peut en revanche induire une toxicité aiguë apparaissant chez 80 % des patients dans les heures suivant l’injection (apparition de paresthésies des extrémités et de contractions musculaires), plus particulièrement lors de l’exposition au froid. Moins fréquemment sont décrits des troubles visuels, des paresthésies péribuccales ou des troubles laryngés. Ce tableau, reflet d’une hyperexcitabilité des fibres nerveuses périphériques par blocage des canaux sodiques, est systématiquement réversible sous quelques jours. La prévention est essentielle et repose sur l’utilisation de sels de calcium et de magnésium lors de l’injection de la chimiothérapie, et de mesures d’isolement complet vis-à-vis du froid pendant la séance (et dans les heures qui suivent) : ports de gants, écharpe, couverture ou manteaux, exclusion des boissons et aliments froids, pas d’exposition à une ouverture du réfrigérateur. Le degré de la toxicité aiguë peut prédire la sévérité de la toxicité chronique. • Le type de toxicité du carboplatine est voisine de celle du cisplatine, mais très rare Elle est décrite pour de très hautes doses chez seulement 6 % des patients. Autres agents • Thalidomide La thalidomide est un médicament ancien qui est actuellement utile dans certains myélomes et leucémies myéloblastiques aiguës de l’adulte. L’atteinte du nerf périphérique est fréquente, jusqu’à 81 % des cas dans certaines séries, mais tardive et pour des doses cumulatives habituellement 20 g. Il s’agit d’une polyneuropathie axonale, longueur-dépendante, à nette prédominance sensitive et douloureuse qui le plus souvent ne régresse pas à l’arrêt du traitement. L’atteinte motrice, quand elle existe, est peu sévère. Lors d’une étude récente sur 75 patients avec myélome multiple, la comparaison entre 6 et 12 mois de traitement par thalidomide, montrait une NPCI dans 38 % et 78 % des cas, respectivement. Cette étude démontre également qu’il existe des séquelles électrophysiologiques sensitives, le plus souvent infracliniques, dans 39 % des cas. Neuropathies périphériques et chimiothérapies Vinca-alcaloïdes = alcaloïdes de la pervenche ; CDDP = cisplatine ; IT = intrathécale ; ROT = réflexes ostéo-tendineux. Conduite à tenir devant une NPCI Le traitement préventif des NPCI a été longuement étudié mais dans des petites séries rétrospectives et rarement prospectives. Différents agents (oxcarbamazépine, amifostine, Org 2766, vitamine E, glutathione, glutamine, N-acétylcystéine, L-acétyl-carnithine) ont ainsi été étudiés. Les résultats sont encourageants, mais ces molécules n’ont pas fait l’objet de grandes études randomisées. En pratique, aucun de ces agents n’est utilisé de manière systématique, à l’exception des perfusions IV de calcium pour la prévention des NPCI précoces après traitement par l’oxaliplatine. Les mesures les plus utiles sont symptomatiques : le traitement antidouleur (antiépileptiques et anti dépresseurs) et la physiothérapie. En pratique clinique, la prise en charge d’une neuropathie chez un patient recevant une chimiothérapie neurotoxique dépend de la distribution de l’atteinte neuropathique (symétrique longueur-dépendante vsmultifocale) et du mode d’apparition. Il existe en effet 2 cas de figure, le cas « typique » et « atypique ». Si la NPCI apparaît de manière cohérente dans le temps (pendant les cures de chimiothérapie) et dans l’espace (symétrie du tableau clinique), il n’est pas nécessaire d’effectuer des examens complémentaires et en particulier d’EMG pour retenir le diagnostic de NPCI. Il s’agit ici du cas de figure « typique ». Un traitement symptomatique ne sera proposé que si le patient se plaint de douleurs ou de dysesthésies invalidantes. Le traitement symptomatique n’est pas nécessaire dans le cadre de paresthésies à type d’engourdissements ou de fourmillements. Son efficacité n’a jamais été démontrée dans cette indication. L’apparition de la neuropathie est en revanche « atypique » lorsqu’elle survient à distance de l’arrêt de toute chimiothérapie, lorsque la distribution clinique est non compatible avec la toxicité de la drogue utilisée ou sans caractère symétrique, ou lorsque des signes centraux ou des nerfs crâniens sont associés. Il est alors indiqué de demander un avis neurologique et d’effectuer un bilan complémentaire simple, à commencer par une prise de sang et un EMG, qui pourra être en faveur d’une NPCI en retrouvant des anomalies électrophysiologiques symétriques ou encore qui orientera vers un autre type de neuropathie nécessitant de rechercher en premier lieu une cause infiltrative, compressive, carentielle ou paranéoplasique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :