Publié le 16 avr 2009Lecture 15 min
Quelle prise en charge précoce des hémorragies méningées par rupture d'anévrysme ?
T. LESCOT, L. ABDENNOUR, L. PUYBASSET, Unité d’anesthésie et de réanimation neurochirurgicale, Département d’Anesthésie Réanimation, Groupe hospitalier Pitié-Salpêtrière et Université Pierre et Marie Curie (Paris VI), Paris
Cause la plus fréquente d’hémorragie méningée, la rupture d’anévrysme intracérébral reste grevée d’une mortalité lourde et d’un risque de séquelles important n’épargnant que 20 % des patients traités. L’amélioration du pronostic passe par une prise en charge en urgence dans un centre de référence, où pourra être réalisé au cas par cas un traitement curatif de l’anévrysme par voie endovasculaire ou chirurgical.
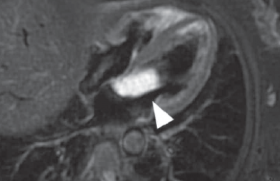
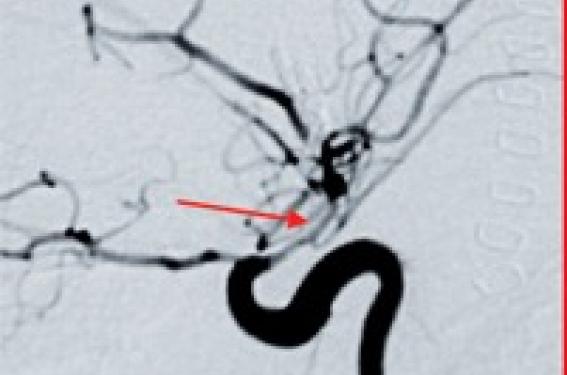
L’ hémorragie méningée anévrysmale correspond à la rupture d’un anévrysme artériel intracrânien responsable de l’irruption de sang dans les espaces sous-arachnoïdiens. Les différentes études épidémiologiques estiment que l’incidence de cette pathologie est comprise entre 4,5 et 28 pour 100 000 habitants et par an (1) pour une prévalence d’anévrysme non rompu au sein de la population générale évaluée entre 0,5 et 6 %, selon les méthodes (angiographiques ou nécroscopiques) de recueil des données. La population concernée est jeune, le pic d’incidence étant maximal entre 30 et 60 ans. Environ 12 % des patients décèdent avant toute prise en charge médicale (2). Un an après avoir bénéficié d’une cure anévrysmale, 10 % des patients sont décédés, 18 % restent porteurs de séquelles lourdes et invalidantes, et seuls 20 % des patients ne présentent aucune séquelle (3). Le resaignement précoce et le vasospasme et ses conséquences sont responsables d’une grande partie des évolutions défavorables. Environ 12 % des patients décèdent avant toute prise en charge médicale. Physiopathologie L'hémorragie méningée anévrysmale est définie par l'irruption de sang dans les espaces sous-arachnoïdiens à partir de la fissuration d'une paroi artérielle anormale. Cette dysplasie artérielle congénitale (absence ou atrophie des couches élastiques et musculaires de l'intima) se rencontre le plus souvent au niveau des gros vaisseaux intracrâniens de la base du crâne et plus particulièrement au niveau de leurs bifurcations. Avec le temps et sous les effets de la pression artérielle, la paroi vasculaire dysplasique se distend progressivement et se boursoufle pour aboutir à la formation d'un anévrysme. Dans 80 % des cas environ, ils touchent la circulation cérébrale antérieure : terminaison de l’artère carotide interne, artère communicante antérieure, artère péricalleuse, artère cérébrale moyenne (4). Classiquement, cet anévrysme est constitué d'un sac et d'un collet, les formes atypiques fusiformes, polylobées n'étant pas rares de même que les localisations multiples observées dans 20 à 30 % des cas. Lors de la rupture anévrysmale, l’issue brutale de sang entraîne une augmentation rapide de la pression intracrânienne (PIC). La formation d’un caillot intra-anévrismal, favorisé par l’augmentation de la PIC (et donc la diminution du gradient de pression transanévrysmal), empêche la poursuite du saignement. La diminution de la PIC permet secondairement la restauration d’une PPC compatible avec un retour à la conscience. C’est l’évolution habituellement observée chez les patients en grades I et II de la classification de la World Federation of Neurosurgeons (WFNS – tableau 1) présentant un tableau clinique peu sévère. En cas d’hémorragie méningée massive, d’inondation ventriculaire, d’hématome intraparenchymateux ou d’hypotension artérielle, la faillite des mécanismes de compensation aboutit à la persistance d’une hypertension intracrânienne (HTIC), et se traduit alors cliniquement par des troubles de la conscience et/ou l’existence d’un déficit moteur : grades III, IV et V de la classification de la WFNS, dont les taux de mortalité et de morbidité sont alors considérablement augmentés (5). Le niveau de la PIC est corrélé au grade clinique du patient : normale ou légèrement élevée chez les patients en grades I et II, et habituellement élevée voire très élevée chez les patients en grades IV et V6. Présentation clinique Le diagnostic est le plus souvent facile, car le tableau clinique est très souvent évocateur : céphalée brutale qui survient le plus souvent au cours d'un effort (coït, défécation, activité sportive), fréquemment accompagnée de nausées, de vomissements et d’un syndrome méningé. Les troubles de la conscience sont variables, soit absents, soit le plus souvent présents, de la simple obnubilation au coma profond. L'apparition brutale de ce tableau chez un sujet jeune, auparavant en bonne santé, est très évocatrice d'hémorragie méningée anévrysmale. Les signes neurologiques focaux ne sont pas rares. Ils peuvent être présents d'emblée, évocateurs d'un hématome intracérébral associé, ou apparaître secondairement et, dans ce cas, plus évocateurs d’un vasospasme si le patient est vu plusieurs jours après le premier épisode de saignement. L'hémiplégie est de diagnostic facile, mais il faut s'attacher à retrouver également une aphasie, une hémianopsie, des troubles sensitifs, dont le diagnostic est difficile chez les patients confus. Examens complémentaires Scanner cérébral Le scanner cérébral sans injection de produit de contraste reste le premier examen à réaliser en urgence devant toute suspicion d’hémorragie méningée. Il permet d’établir le diagnostic positif en mettant en évidence une hyperdensité spontanée des espaces sous arachnoïdiens. Le scanner offre également la possibilité d’évaluer l’importance de cette hé-morragie que l’on peut apprécier par la classification de Fisher (tableau 2). Enfin, son interprétation s’attachera également à rechercher une complication cérébrale initiale : hydrocéphalie, hématome, infarctus. En cas de doute d’interprétation, les images doivent faire l’objet d’une télétransmission vers un centre de référence. Le scanner se normalise en quelques jours par effet de lavage du liquide céphalorachidien (LCR). Ainsi, plus le scanner est réalisé précocement, plus cet examen est sensible. Un scanner normal n’élimine en aucun cas le diagnostic d’hémorragie méningée, et impose la réalisation d’une ponction lombaire atraumatique, par un opérateur entraîné. Le recueil de liquide céphalorachidien clair élimine définitivement le diagnostic. À l’inverse, la présence de liquide céphalorachidien xanthochromique et incoagulable témoigne d’une hémorragie méningée. Toute dégradation neurologique impose la réalisation d’un nouveau scanner. Un scanner normal n’élimine en aucun cas le diagnostic d’hémorragie méningée. L’angioscanner avec reconstruction tridimensionnelle prend une place croissante pour préciser le collet et les rapports de l’anévrysme avec les structures vasculaires adjacentes. Cependant, cet examen n’a qu’un intérêt préthérapeutique et n’est donc pas utile pour la décision du transfert du patient. Imagerie par résonance magnétique L’imagerie par résonance magnétique (IRM), couplée à l’angiographie par résonance magnétique (ARM), est de plus en plus pratiquée en première intention, en particulier chez les patients présentant un scanner cérébral normal et chez lesquels la réalisation d’une ponction lombaire s’avère risquée (prise d’anticoagulants, aspirine). Certaines séquences (FLAIR) sont particulièrement sensibles pour détecter un saignement intracrânien. L’IRM en coupes axiales peut montrer la dilatation anévrismale (vide de signal pour la partie circulante, signal de densité hétérogène dans une partie thrombosée). Les ARM actuelles sont capables d’identifier des anévrysmes de quelques millimètres avec une sensibilité de près de 80 %. Angiographie cérébrale Figure 1. Tomodensitométrie (A), angio-tomodensitométrie (B) et artériographie (C) montrant une hémorragie méningée secondaire à la rupture d’un anévrysme artériel de la terminaison carotidienne gauche. Le diagnostic d’hémorragie méningé établi, son étiologie sera précisée grâce à la réalisation, en urgence, d’une angiographie cérébrale (figure 1). Elle sera alors effectuée dans le premier temps du traitement endovasculaire. Elle comporte une étude des quatre axes nourriciers du polygone de Willis (artères carotides et vertébrales + tronc basilaire), avec des incidences multiples. Elle met en évidence l’anévrysme artériel (image d’addition opacifiée aux temps artériels précoces), précise son volume, ses rapports avec les axes vasculaires, sa forme et le siège du collet. Elle est parfois normale malgré l’existence d’un anévrysme (partiellement thrombosé ou masqué par le vasospasme associé), et sera alors rediscutée 6 à 8 semaines après les céphalées si les signes cliniques étaient typiques en dehors des hémorragies strictement prépontiques. Dosage de la protéine S100-β La protéine S100-β est sécrétée par le système nerveux central, et peut être retrouvée dans le plasma après lésion de la barrière hémato-encéphalique. Sa concentration est corrélée à la gravité de l’atteinte cérébrale au cours des hémorragies méningées anévrysmales. Son dosage quotidien permet un dépistage des lésions ischémiques secondaires et doit faire aujourd’hui parti du monitorage des patients présentant une hémorragie méningée anévrysmale (HMA) (7). Traitement Tout patient présentant une hémorragie méningée anévrysmale doit être hospitalisé dans un centre de référence comprenant neurochirurgiens, neuroréanimateurs et neuroradiologues (8). Ils doit être pris en charge en neuroréanimation ou dans une réanimation polyvalente ayant une compétence spécifique en neuroréanimation. La prise en charge pluridisciplinaire a pour but d’éviter les complications précoces ou de les traiter et de prévenir voire traiter le vasospasme. Un traitement de réanimation intensif des patients en grade élevé (monitorage de la PIC, drainage du LCS, monitoring hémodynamique, triple H thérapie précoce) améliore significativement leur pronostic. Tout patient présentant une hémorragie méningée anévrysmale doit être hospitalisé dans un centre de référence. Traitement du sac anévrysmal Le traitement curatif précoce de l’anévrysme visualisé à l’angiographie cérébrale consiste à exclure le sac anévrysmal de la circulation cérébrale, soit chirurgicalement, soit par procédure endovasculaire (9). La décision du choix thérapeutique doit résulter d’une discussion entre chirurgiens, radiologues et neuro-anesthésistes. Celle-ci doit tenir compte de la localisation de l’anévrysme, de son aspect morphologique, de l’état clinique du patient et de ses antécédents. La disponibilité et l’expérience des équipes chirurgicale et neuroradiologique sont des critères qui interviennent dans la discussion. ■ Traitement endovasculaire C’est le traitement recommandé lorsqu’il est techniquement possible. Son objectif est d’occlure l’anévrysme par des coils largables, introduits par voie endovasculaire, dans le sac anévrysmal. Ce traitement se déroule en deux phases : microcathétérisme du sac anévrysmal et occlusion de la poche anévrysmale. Les limitations des indications du traitement endovasculaire tiennent avant tout à la taille du collet. ■ Traitement chirurgical des anévrysmes intracrâniens En cas d’engagement cérébral et si la localisation de l’hématome au scanner est suffisamment informative, le traitement chirurgical de l’anévrysme peut être réalisé sans angiographie diagnostique, car dans ces formes graves, le pronostic dépend de la précocité du traitement chirurgical qui consiste en la pose d’un clip sur le collet de l’anévrysme, précédé d’une évacuation de l’hématome. ■ Abstention Parfois, une abstention thérapeutique sera choisie si les lésions cérébrales initiales consécutives à la rupture anévrysmale sont trop importantes, ou si le patient présente des signes de gravité extrêmes (engagement cérébral) dans un contexte de coma profond. Complications Vasospasme artériel cérébral Le vasospasme artériel cérébral constitue l’une des complications les plus graves de l’hémorragie méningée anévrysmale. Sa survenue serait responsable d’une multiplication par deux du taux de mortalité dans les 2 semaines suivant la rupture anévrysmale. Le vasospasme est d’autant plus fréquent que le patient présente un grade de Fisher élevé, un haut grade clinique (WFNS) et une atteinte myocardique avec bas débit. Cette complication survient préférentiellement entre le 4e et le 12e jour d’évolution. Sa physiopathologie reste obscure. Figure 2. Vasospasme artériel de la terminaison carotidienne (A, flèche). Effets de l’injection intra-artérielle in situ de nimodipine permettant une restauration du diamètre vasculaire (B). Sa prévention repose sur l’utilisation de la « triple H thérapie » associant hypertension artérielle, hémodilution et hypervolémie. Le traitement hyperdynamique est administré en réanimation, sous monitorage continu approprié, comportant au minimum la mesure invasive de la pression artérielle et de la pression veineuse centrale. L’administration de nimodipine est systématique pendant 21 jours, par voie intraveineuse ou bien per os. Le diagnostic de vasospasme est suspecté devant l’apparition d’une fièvre, de troubles de la conscience, d’un déficit moteur ou sensitif, associés à une accélération des vélocités moyennes de l’artère cérébrale moyenne (> 120 cm.s-1) au Doppler transcrânien (10). Ce tableau impose la réalisation d’un scanner cérébral en urgence (qui éliminera une ischémie cérébrale constituée, une hydrocéphalie, un hématome intraparenchymateux ou un resaignement), puis d’une angiographie cérébrale. Celle-ci reste l’examen diagnostic de référence et permet également d’effectuer, en l’absence d’ischémie cérébrale, un traitement endovasculaire de type mécanique (angioplastie) ou pharmacologique (nimodipine, milrinone, donneurs de NO) (figure 2). Hypertension intracrânienne et hydrocéphalie aiguë L’hémorragie méningée anévrysmale s’accompagne fréquemment d’une hypertension intracrânienne chez les patients en grade clinique élevé, et résulte le plus souvent d’un ou de plusieurs des mécanismes suivants : - un hématome intracérébral peut accompagner une hémorragie méningée anévrysmale dans 20 % des cas et être directement responsable d’une HTIC. Dans ce cas, l’évacuation est chirurgicale et suivie de la cure de l’anévrysme ; - un oedème cérébral peut s’installer dans les heures qui suivent l’hémorragie méningée anévrysmale. Il impose un monitorage de la pression intracrânienne, au mieux par cathéter intraventriculaire permettant une soustraction de liquide céphalorachidien ; - une hydrocéphalie résultant du trouble de la résorption du liquide cérébro-spinal, du fait du sang présent dans les espaces sous-arachnoïdiens, peut survenir rapidement. Elle impose une dérivation ventriculaire externe (DVE) en urgence. Un hématome intracérébral peut accompagner une hémorragie méningée anévrysmale dans 20 % des cas. Resaignement précoce L’objectif premier du traitement de l’anévrysme est d’éviter la récidive hémorragique par une exclusion précoce. Le resaignement à un taux de mortalité de plus de 70 %. C’est la raison pour laquelle les anévrysmes doivent être traités dans les 48 premières heures. Épilepsie La majorité des convulsions sont précoces et associées à un mauvais pronostic neurologique. Aucune donnée formelle ne permet de statuer sur la prophylaxie antiépileptique. Une prophylaxie antiépileptique peut être envisagée en présence d’un hématome, d’un infarctus cérébral ou d’une lésion focale. Répercussions cardiovasculaires et pulmonaires Les hémorragies méningées anévrysmales peuvent entraîner des troubles du rythme cardiaque, des altérations de la fonction myocardique et un oedème pulmonaire. Dans les cas les plus graves, l’oedème pulmonaire « neurogénique » aboutit à un syndrome de détresse respiratoire aigu compliquant la prise en charge de la pathologie anévrysmale. Des anomalies électrocardiographiques sont également présentes dans 50 % des cas au décours d'une rupture d’anévrysme. Des anomalies du rythme et de la conduction à l'étage supraventriculaire et ventriculaire sont fréquemment observées. Les troubles de la repolarisation ne sont pas rares et peuvent suggérer l’existence d’une souffrance myocardique. Complications tardives Hydrocéphalie Une hydrocéphalie peut survenir dans les semaines qui suivent la rupture anévrysmale. Elle est liée à la fibrose des espaces sous-arachnoïdiens et à une prolifération inflammatoire des cellules des villosités arachnoïdiennes. Elle est plus fréquente chez les patients en grade élevé (WFNS). Au plan clinique, les troubles de la conscience et les troubles psychiatriques organiques dominent. C’est une hydrocéphalie communicante qui nécessitera la mise en place d’une dérivation ventriculo-atriale ou ventriculo-péritonéale, et peut transitoirement être traitée par la réalisation de ponctions lombaires évacuatrices. Reperméation du collet Une reperméation de l’anévrysme est possible au niveau de son collet. Son incidence est devenue faible avec les nouveaux matériaux d’embolisation. Néanmoins, sa recherche impose la réalisation d’ARM de contrôle chez les patients embolisés. La fréquence de ces examens ira en décroissant avec le temps, en cas de normalité. Pronostic Il est souvent avancé que 20 à 30 % des patients victimes d’une hémorragie méningée anévrysmale meurent à domicile. Les patients arrivant en grade I ou II de la classification de la WFNS ont une probabilité d’avoir peu ou pas de séquelles à un an, qui dépasse 90 %. Cependant, la mortalité dans ce groupe n’est pas nulle. Le pronostic est beaucoup moins bon pour les grades IV et V : de l’ordre de 40 à 50 % pour les grades IV et de 20 à 30 % pour les grades V.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :