Pathologie vasculaire
Publié le 03 déc 2018Lecture 16 min
Écho-Doppler transcrânien - Pathologie athéromateuse intracrânienne
Ghislaine DEKLUNDER, Corinne GAUTIER, Service d’explorations fonctionnelles cardiovasculaires, Hôpital cardiologique, Centre hospitalier régional et universitaire, Lille
L’exploration des artères cérébrales dans leur trajet intracrânien n’est pas toujours systématique en présence d’une ischémie cérébrale. Elle est pourtant tout aussi importante que l’exploration de ces artères dans leur segment cervical. En effet, elle permet à la fois d’évaluer le retentissement des lésions cervicales et de dépister l’existence de lésions artérielles intracrâniennes associées. Les conséquences pratiques sont majeures puisque l’attitude thérapeutique dépend de l’ensemble de ces données. Si l’usage n’en est pas jusqu’ici généralisé, l’écho-Doppler transcrânien doit donc devenir partie intégrante du bilan d’une ischémie cérébrale. Les limitations techniques de l’examen peuvent presque toujours être surmontées à l’heure actuelle par l’utilisation d’un agent de contraste ultrasonore, ce qui devrait favoriser grandement le recours plus large à cette exploration.
Données générales sur l’athérome intracrânien
L’athérosclérose intracrânienne est considérée comme responsable de 8 à 10 % des accidents ischémiques cérébraux (AIC) dans les pays occidentaux. La prévalence est beaucoup plus élevée dans les populations d’origine hispanique, africaine ou asiatique, et peut atteindre 40 % chez les asiatiques(1-4).
L’âge, l’hypertension, le diabète et le syndrome métabolique, de même que la coexistence d’une maladie coronaire, sont les plus souvent cités(4,5). Les facteurs de risque sont les mêmes, quel que soit le territoire intracrânien concerné. Il n’y a pas de différence de prévalence entre les sexes(2).
L’utilisation croissante de l’exploration du polygone de Willis, en EDTC ou en ARM, montre clairement que la fréquence de l’athérome intracrânien est bien plus élevée que celle classiquement décrite(2,5). Le peu d’intérêt apporté antérieurement à ces lésions était essentiellement lié au fait que seule l’angiographie en permettait le diagnostic et qu’aucune action thérapeutique spécifique n’était envisageable.
La localisation de l’athérosclérose n’est pas uniforme sur les artères intracrâniennes et on observe, comme dans tous les autres territoires artériels, des sites lésionnels de prédilection. Les artères les plus souvent concernées sont les artères du territoire postérieur, artères vertébrales (AV) en V4 et artère basilaire (AB) (40 à 48 % des localisations selon les séries). Viennent ensuite l’artère carotide intracrânienne (ACI) (25 à 30 %) avec, par ordre de fréquence décroissante, la portion caverneuse, la portion intra-pétreuse, et enfin le segment clinoïdien, puis l’artère cérébrale moyenne (ACM) dans son segment M1 (20 à 26 %)(2,5). Le Groupe d’étude des sténoses intracrâniennes athéromateuses symptomatiques (GESICA) a cependant montré dans une étude prospective que la répartition était en réalité assez homogène et que les AV, AB, ACM et ACI étaient concernées avec une fréquence à peu près similaire(6). Il faut également noter que l’athérome intracrânien est souvent diffus et qu’il existe donc fréquemment des localisations multiples, l’association de lésions athéroscléreuses du système carotidien et du système vertébrobasilaire n’est donc pas rare(3,4).
En présence d’une lésion athéromateuse intracrânienne, la prise en charge actuelle est la suivante :
- contrôle extrêmement rigoureux des facteurs de risque ;
- utilisation d’un traitement médical renforcé ;
- recours à l’angioplastie avec le plus souvent pose de stent, dans certaines conditions tout au moins (sténose > 70 %, accessibilité de la lésion, contexte général).
La situation devient par voie de conséquence radicalement différente(3). Le succès technique de l’angioplastie est actuellement assuré dans les équipes expérimentées et le taux de complications est faible (environ 5 %), le bénéfice à long terme reste cependant à démontrer(1,4).
Le territoire carotidien
Le siège le plus fréquent de l’athérome sur l’ACI est certes le bulbe de la carotide interne cervicale, mais le siphon carotidien vient en 2e position. Les plaques prédominent sur les concavités internes du siphon. Les sténoses du siphon carotidien représentent environ 15 à 20 % des sténoses carotidiennes, elles sont plus fréquentes et plus sévères que les sténoses du segment intrapétreux de la carotide interne(7). L’athérosclérose peut aussi affecter le segment M1 de l’artère cérébrale moyenne et le segment A1 de l’artère cérébrale antérieure.
Les lésions associées, dites en tandem, touchant à la fois le bulbe carotidien et le siphon, ont une prévalence estimée à 8 % dans une population à risque vasculaire élevé. La coexistence d’une lésion intracrânienne, toutes localisations confondues, et d’une lésion cervicale asymptomatique, peut concerner jusque près de 30 % de ces patients(5).
L’histoire naturelle de l’athérosclérose de la carotide intracrânienne est moins bien connue que celle de la localisation cervicale, mais le risque de morbimortalité cérébrovasculaire lié à un infarctus cérébral ispsilatéral à la sténose semble comparable puisqu’il est en effet estimé globalement à 3 % par an. Cependant, si on regarde les statistiques en détail, il apparaît que cette évaluation moyenne couvre d’importantes disparités puisque les sténoses asymptomatiques de l’ACM ont un bon pronostic à long terme, avec un faible risque d’AIC ischémique ipsilatéral sous traitement médical optimal, mais que les sténoses de la terminaison de l’ACI et les sténoses symptomatiques serrées (> 70 %) ont, malgré un traitement médical bien conduit, un risque élevé d’instabilité et donc d’événement clinique (récidive à 2 ans de 15 à 38 %, selon la classe de risque)(1,4,6,8).
Le territoire vertébro-basilaire
De même que pour le système carotidien, ce sont les segments extracrâniens qui sont le plus souvent affectés, mais avec cette fois un risque faible d’infarctus cérébral. Comme il a été dit plus haut, les segments intracrâniens les plus touchés par l’athérosclérose sont l’artère vertébrale dans son segment V4, et l’artère basilaire dans son segment proximal. L’athérosclérose de V4 et de l’AB semble entraîner un risque très élevé d’ischémie cérébrale(8,9). Il est regrettable que, pour l’instant, le risque de complications de l’angioplastie soit également le plus élevé dans ces vaisseaux.
Il n’est pas surprenant de constater que les conséquences des sténoses vertébrales sont d’autant plus sévères qu’il existe une franche asymétrie de calibre et que la sténose siège sur l’artère vertébrale dominante. En ce qui concerne les lésions de l’artère basilaire, les sténoses serrées sont le plus souvent localisées dans la moitié proximale de l’artère, avec des conséquences d’autant plus sévères que la lésion est très proximale. Les branches de division de l’artère basilaire, artères perforantes paramédianes, artères circonférentielles courtes et artère cérébelleuse antéro-inférieure, peuvent, elles aussi, être affectées(10).
Détection de l’athérome intracrânien
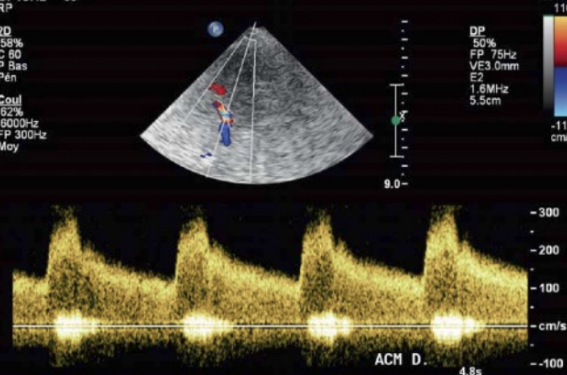
La sémiologie d’une sténose intracrânienne n’a rien de spécifique et se caractérise, comme dans n’importe quel territoire, par la présence d’une accélération focale des vitesses repérée en raison d’un repliement spectral focal en Doppler couleur puis analysée en Doppler spectral (figure 1). Cette analyse permet de mesurer les vitesses circulatoires et démontre également la redistribution de l’énergie spectrale. Les sténoses athéromateuses intracrâniennes siégeant le plus souvent à l’origine des gros vaisseaux, ces zones doivent être très soigneusement étudiées lorsqu’on suspecte leur existence. En cas de sténose serrée, il faut aussi rechercher la présence de signes d’amont et d’aval dans le territoire concerné (augmentation des résistances en amont et amortissement des flux en aval). Ces signes aident à connaître le retentissement hémodynamique de la lésion mais ils sont aussi très utiles lorsque les signes directs ne sont pas francs (mauvais alignement du tir Doppler, conditions techniques difficiles). Pour ce faire, il est indispensable de visualiser les vaisseaux sur une certaine longueur et le recours aux agents de contraste est donc fréquent.
Figure 1. Sténose d’une ACM, signes directs : enregistrement spectral sur la zone d’accélération repérée en Doppler couleur. DR
Comme souvent, l’importance du retentissement dépend non seulement de la sévérité de la lésion, mais aussi du développement des voies de suppléance. Il est donc important d’analyser le calibre des vaisseaux susceptibles d’être impliqués dans ces suppléances, le sens circulatoire ainsi que les vitesses en présence, pour infirmer ou affirmer leur mise en jeu.
Un des intérêts majeurs de l’EDTC par rapport au DTC, et de l’utilisation du contraste quand cela s’avère nécessaire, est de permettre la visualisation de l’ensemble du trajet des artères et donc de vérifier le caractère focal ou diffus d’une accélération et de guider de façon adéquate l’enregistrement spectral : positionnement de la zone d’échantillonnage, alignement du tir Doppler dans l’axe de l’écoulement sanguin de façon à n’avoir à utiliser qu’une faible correction angulaire et enfin, quand elle s’avère nécessaire, correction adaptée à la direction réelle du flux(11,12).
Le diagnostic différentiel principal est l’existence d’un hyperdébit compensateur au sein d’une artère impliquée dans une suppléance. L’hyperdébit dans un vaisseau, et ce d’autant que son calibre est en général petit, entraîne en effet accélération et turbulences. Dans ce cas, les anomalies sont cependant observées sur tout le trajet du vaisseau concerné. Une fois de plus, il faut donc souligner l’importance d’une étude exhaustive des artères concernées et se méfier d’une anomalie détectée sur un segment artériel très court, sans exploration possible de l’ensemble du trajet artériel.
Les études comparatives entre anomalies ecueillies en DTC(13), en EDTC(14,15) et en angiographie, ont permis de déterminer des critères de sténose. La quantification repose sur la mesure de la vitesse maximale systolique (VMS) mesurée au site de la sténose, avec une correction angulaire si l’abord ne permet pas un alignement optimal du tir Doppler. On ne dispose pas de critères de quantification précis pour l’ensemble des segments artériels. Les valeurs seuil permettent simplement de séparer les sténoses supérieures ou inférieures à 50 % (VMS respectivement ≥ 120 et ≥ 155 cm/s pour l’ACA ; ≥ 100 et ≥ 145 cm/s pour l’ACP et l’AB ; ≥ 90 et ≥ 120 cm/s pour l’AV)(5,14,15). En ce qui concerne l’ACM, une classification plus précise a été retenue : sténose < 50 % VMS entre 140 et 209 cm/s, sténose entre 50 et 70 % VMS entre 210 et 279 cm/s, sténose > 70 % VMS > 280 cm/s(15,16).
Ces critères ne s’appliquent cependant que lorsque l’on est en présence d’une sténose focale unique sans lésion associée des artères à l’étage cervical, en l’absence d’hypoplasie, lorsqu’il n’y a pas de suppléance mise en charge (ce qui est toujours le cas pour certains segments comme M1, M2, A2, P2, P3, pour lesquels aucune suppléance n’est possible) et chez un patient dont la fonction cardiaque est normale(2,14).
L’angiographie reste pour l’instant le « gold standard » même si en pratique la place de l’ARM et de l’EDTC est devenue très importante(12,15). Il est regrettable que peu de séries comparant les données de l’EDTC à celles de l’ARM soient disponibles à ce jour(16).
La sémiologie des occlusions paraît toujours simple puisqu’il suffit d’affirmer l’absence de flux dans un vaisseau ou dans un segment de vaisseau. En pratique l’exercice est souvent difficile, a fortiori en exploration intracrânienne, puisque les difficultés techniques et les variations anatomiques sont fréquentes dans ce territoire vasculaire. L’utilisation des produits de contraste ultrasonore (PCUS) a permis de s’affranchir des problèmes d’accès et d’améliorer ainsi considérablement les performances de l’EDTC dans ce diagnostic.
Une occlusion se caractérise par l’absence de signal Doppler en mode couleur, puissance et spectral. Elle n’est affirmée qu’après recours à un PCUS. La longueur de l’occlusion doit être précisée. Les signes indirects varient selon le site de l’occlusion et sont essentiellement fonction de la capacité de mise en jeu de suppléances (qui dépend elle-même de la localisation de l’occlusion ainsi que de la qualité des axes susceptibles de servir de voie collatérale). Par exemple, en cas d’occlusion de l’ACI intracrânienne, les vitesses seront basses et le niveau des résistances sera augmenté dans l’ACI cervicale seulement si l’occlusion se situe en amont de la naissance de l’artère ophtalmique. De même, en présence d’une occlusion distale de l’AB, les flux des AV et de l’AB proximale ne seront altérés que si les collatérales (AICA et perforantes) ne peuvent être recrutées.
Limites, pièges et solutions
L’aspect souvent sinueux des artères intracrâniennes peut rendre difficile la mesure des vitesses absolues pourtant indispensables à la quantification des sténoses. Une mesure de vitesse n’est en effet réalisable que si le segment artériel étudié présente un trajet rectiligne bien identifié suffisamment long (> 15 mm), ce qui permet d’appliquer une correction angulaire quand elle s’avère nécessaire. Dans le cas contraire, les anomalies spectrales pourront évoquer la sténose, sans qu’il soit possible de l’affirmer et a fortiori de la quantifier(2,15). Aborder le vaisseau avec un angle de tir Doppler favorable est particulièrement difficile au niveau du siphon carotidien. C’est la raison pour laquelle certains auteurs préconisent l’utilisation, en complément des coupes axiales de référence, de coupes coronales avec des résultats très satisfaisants (100 % de succès pour l’ensemble des segments à l’exception de la partie horizontale de C6 pour laquelle le succès n’est au rendez-vous « que » dans 97 % des cas)(17,18). Ces coupes peuvent aussi être utiles pour dégager complètement l’AB, par voie temporale ou par voie foraminale.
En cas de suspicion de sténose, lorsqu’il n’est pas possible d’analyser l’artère sur un trajet suffisamment long pour affirmer le caractère focal de l’anomalie, il peut être utile de comparer les vitesses mesurées en un site à celles du même site controlatéral. En raison de l’existence de nombreuses variantes anatomiques et des asymétries fréquentes de calibre entre les deux côtés pour une même artère, cette comparaison des vitesses entre les côtés droit et gauche n’a de réelle valeur que pour les ACI, les ACM et les segments P2 et P3 des ACP qui sont le plus souvent symétriques d’un point de vue anatomique.
De même que pour les autres territoires artériels de l’organisme, pour éviter les pièges liés aux modifications de l’hémodynamique générale, il est indispensable de comparer les vitesses au site de la sténose à celles présentes en amont, sur l’ACI cervicale en aval du bulbe. Jusqu’ici, aucune recommandation n’a cependant été rapportée quant aux seuils de rapports de vitesses à prendre en considération pour la quantification. En pratique, on utilise donc par analogie les mêmes valeurs que dans les autres territoires (sténose 50 à 69 % ratio entre 3 et 4, sténose > 70 % ratio > 4).
Quoi qu’il en soit, il est toujours indispensable d’explorer à la fois les segments cervicaux et intracrâniens des artères encéphaliques pour pouvoir interpréter correctement la sémiologie Doppler. En effet, si l’on méconnaît une sténose significative au cou, le risque de sous-estimation de la sténose intracrânienne est important. En ce qui concerne les artères vertébrales, il importe de connaître le calibre de leurs segments proximaux puisqu’à la fois le calibre, les vitesses circulatoires et même le trajet du segment V4 leur est lié.
Méthode d’examen
Il convient de débuter l’examen par un écho-Doppler cervical pour les raisons évoquées plus haut, et de réaliser ensuite l’EDTC. L’exploration débute en général par le côté supposé sain de façon à avoir des vitesses de référence pour chaque segment artériel (voir « L’écho-Doppler transcrânien. Exploration artérielle (examen normal) » EDV 2009 ; 2 : 16-19).
En utilisant le mode couleur, on vérifie la perméabilité des différents segments artériels, le sens circulatoire et on recherche, sur chacun des segments, des anomalies focales de vitesse, se manifestant par une zone de repliement spectral. La PRF doit être adaptée aux conditions hémodynamiques du patient, il ne faut pas hésiter à la faire varier au cours de l’exploration pour pouvoir :
- visualiser correctement à la fois les segments proximaux et distaux d’une artère donnée (la vitesse étant plus basse dans le segment distal) ;
- identifier successivement la zone de sténose où les vitesses sont élevées et le flux d’aval où les vitesses peuvent par contre être basses s’il existe un retentissement hémodynamique ;
- affirmer une occlusion : différentier une sténose très serrée (débit non maintenu, absence d’accélération, vitesses basses) d’une occlusion.
L’étude doit bien entendu être la plus complète possible et concerner les segments proximaux et distaux des artères, en effectuant, pour chaque segment, une comparaison des vitesses entre les côtés droit et gauche. Quand une accélération est présente, il faut toujours classer la sténose au moins comme < ou ≥ 50 % et plus précisément en ce qui concerne l’ACM selon les seuils décrits plus haut, en raison de l’impact thérapeutique qui en découle(15,16,19). L’analyse exhaustive permet aussi de détecter la présence de branches collatérales anormalement développées.
À la fin de l’examen, la localisation, la sévérité de la (des) sténose(s), la présence d’un segment occlus ainsi que le retentissement hémodynamique des lésions doit être précisé dans le compte rendu. Le recours à un PCUS, s’il s’est avéré nécessaire, doit être mentionné.
Il n’y a pas de consensus quant au rythme de surveillance à adopter lorsqu’une lésion athéromateuse intra- crânienne a été détectée. En pratique, l’examen est répété une fois par an ou par 6 mois en fonction de la sévérité de la lésion, de la tolérance clinique et du contexte, que l’on ait opté pour un trai- tement médical ou pour un traitement endovasculaire.
Même si la place de l’EDTC va croissant, une évaluation multimodale des sténoses intracrâniennes est recommandée(2,11,14,20). L’IRM de l’encéphale est toujours réalisée pour le bilan des lésions parenchymateuses et souvent l’ARM y est associée car, même si la quantification des lésions semble moins précise qu’en angioscanner, elle ne prolonge pas de beaucoup la durée de l’examen et fournit une bonne imagerie du polygone. En cas de suspicion de sténose en EDTC ou en ARM, et en fonction de l’ensemble des données cliniques et des possibles conséquences thérapeutiques, un angioscanner puis une éventuelle artériographie à but thérapeutique seront parfois effectués. L’intérêt majeur de l’EDTC est de fournir, en plus du diagnostic de la sténose, des données fonctionnelles (retentissement hémodynamique de la lésion, mise en jeu des suppléances et éventuellement étude de la réserve vasomotrice)(2,21).
L’EDTC est parfois susceptible de donner des éléments d’orientation étiologique . L’exemple le plus courant est celui de l’évolution favorable d’une sténose intracrânienne serrée ou d’une occlusion vers la régression ou la disparition totale, spontanée ou obtenue sous traitement médical, qui plaide pour la nature embolique de l’obstacle. Au contraire, la persistance de la sténose dans le temps est bien sûr un argument en faveur de la présence d’une lésion athéromateuse sous-jacente. La répétition de l’EDTC est donc souvent utile (figure 2).
Figure 2. Occlusion d’une ACM. A : signes directs : absence de signal dans l’ACM en Doppler puissance en faveur d’une occlusion (les autres pédicules sont correctement visualisés, ce qui témoigne de réglages adaptés) ; B : l’enregistrement Doppler couleur après thrombolyse montre une bonne recanalisation avec une sténose résiduelle probable (repliement spectral malgré une PRF élevée) ; C : enregistrement spectral après thrombolyse : anomalies mineures, sténose résiduelle non significative. DR
Indications de l’échographie de contraste
Le domaine clinique dans lequel l’extension du champ d’applications de l’échographie vasculaire doit le plus à l’usage des PCUS est pour l’instant la pathologie neurovasculaire. C’est également le seul domaine où l’utilisation des agents de contraste est clairement recommandée(22,23). Quelle que soit l’indication de l’écho-Doppler transcrânien, on aura toujours recours à l’injection d’un agent de contraste lorsque la fenêtre acoustique est mauvaise et que les structures anatomiques sont mal visualisées en 2D, ou lorsqu’il est nécessaire d’effectuer une exploration exhaustive des artères intracrâniennes même si les conditions d’examen sont initialement bonnes(22,24,25).
En pratique, on injecte par voie intraveineuse un bolus de 1 à 2 ml de SonoVue® suivi d’un bolus de 10 ml de sérum physiologique, après avoir optimisé le plan de coupe d’intérêt et l’image. Il est licite d’injecter jusqu’à 4,8 ml, l’injection peut donc être répétée selon l’importance de l’obstacle et du nombre de données à acquérir. Pour tirer un bénéfice optimal du contraste, il est nécessaire d’utiliser un logiciel dédié, ces logiciels sont actuellement disponibles sur la plupart des échographes.
L’injection d’un agent de contraste rend possible l’examen des principales artères intracérébrales chez pratiquement tous les patients. L’identification des variantes anatomiques, extrêmement fréquentes au niveau du polygone de Willis, devient possible, ce qui évite des erreurs grossières d’interprétation. L’utilisation du contraste permet également une exploration plus complète des artères cérébrales, bien au-delà de leur segment proximal, ce qui autorise un examen plus exhaustif, permettant chez la plupart des patients de détecter des sténoses distales, d’analyser leur retentissement et la participation des circuits complexes de suppléance.
L’imagerie des vaisseaux intracrâniens s’impose désormais chez tout patient ayant présenté une ischémie cérébrale. Les avancées technologiques en EDTC et l’utilisation des agents de contraste permettent actuellement une exploration exhaustive des artères cérébrales. C’est la raison pour laquelle l’usage de l’EDTC va croissant, cet examen prend progressivement la place qu’il mérite dans la panoplie diagnostique offerte aux patients.
"Publié dans Cardiologie Pratique"
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :